Daganatkezelés: meg kell állítani a makrofágokat
Általánosan ismert, hogy a rosszindulatú tumor növekedése során makrofágok árasztják el a daganatot. A makrofágok számos gyulladásos és immunszuppressziós mechanizmus révén befolyásolják a tumorfejlődést, ami lehetőséget teremt arra, hogy a hagyományos stratégiák – besugárzás, kemoterápia – mellett más módon is küzdjünk a tumor ellen.
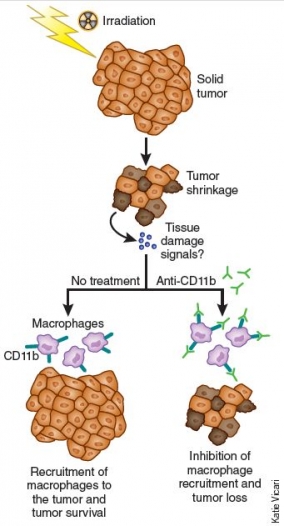
Ahn és munkatársai nemrég igazolták, hogy a makrofágok döntő szerepet játszanak a daganatok besugárzás utáni helyreállásában. Modelljükben a besugárzás után antitestet alkalmaztak egy, a legtöbb makrofág által expresszált sejtfelszíni integrin, a CD11b ellen, és ezzel megakadályozták a makrofágok migrációját a daganat maradványába. A kezeléssel nagyon jó eredményt értek el: a tumor nem növekedett ismét a besugárzást követően. Az ilyen kezelés hasznos adjuváns terápia lehet szolid tumorok esetében.
 A szolid tumorokat nagy számban elárasztó makrofágokat tumor-assszociált makrofágoknak (TAM) nevezik. Számos kutatás keres választ olyan kérdésekre, hogy mi váltja ki a makrofágok felszaporodását a daganatokban, milyen funkciót töltenek be a be a TAM-ok és miként gátolhatók a TAM-ok tumortámogató mechanizmusai. Jelenlegi tudásunk szerint a makrofágok segítik a daganatok növekedését, vagyis káros hatásúak a gazdaszervezetre nézve. Ezt klinikai bizonyítékok is alátámasztják: a makrofágok inváziója rossz kimenetellel jár, főként az emlődaganatok esetében és az emlőrákok egérmodelljeiben.
A szolid tumorokat nagy számban elárasztó makrofágokat tumor-assszociált makrofágoknak (TAM) nevezik. Számos kutatás keres választ olyan kérdésekre, hogy mi váltja ki a makrofágok felszaporodását a daganatokban, milyen funkciót töltenek be a be a TAM-ok és miként gátolhatók a TAM-ok tumortámogató mechanizmusai. Jelenlegi tudásunk szerint a makrofágok segítik a daganatok növekedését, vagyis káros hatásúak a gazdaszervezetre nézve. Ezt klinikai bizonyítékok is alátámasztják: a makrofágok inváziója rossz kimenetellel jár, főként az emlődaganatok esetében és az emlőrákok egérmodelljeiben.
A makrofágok csak teszik a dolgukat...
Más nézőpontból viszont a makrofágok éppen azt teszik, ami elvárható tőlük: a „sérült” (tumorba hatolnak, és az immunszuppresszív környezetben végrehajtják javító-helyreállító funkciójukat. Hasonlóan viselkednek, mint például steril gyulladás (pl. csonttörés, ínsérülés, belső szervi sérülés) esetén: a sérülés helyére gyűlnek, eltávolítják az elpusztult sejteket és a szövettörmeléket, és végül a szövetsérülés begyógyul. Kulcsfontosságú, hogy a szövet, illetve a tumor helyreállítása immunszuppresszív környezetben történjen, mivel igen nagy az esélye a sérült szövet vagy a tumor antigénjei elleni autoimmunitás kialakulásának. A TAM-ok egyik legfontosabb funkciója tehát valószínűleg az immunszuppresszió kialakítása. Ahn és munkatársai egy másik vizsgálata szerint a TAM-ok másik fontos szerepe a gyógyulás egyik részfolyamatának, az érképződésnek a serkentése – revaszkularizáció hiányában a tumor nem indulhatna növekedésnek. Ezt a funkciót az teszi lehetővé, hogy a makrofágok vaszkuláris endoteliális növekedési faktort termelnek, és elősegítik az érhálózatok kialakulását is.
A tumorban felgyűlt makrofágok ellen
A CD11b integrin a legtöbb makrofág és neutrofil leukocita felszínén megtalálható. Ennek – monoklonális antitesttel történő – gátlásával érte el Ahn kutatócsoportja a makrofágok tumorsegítő aktivitásának megszüntetését. Az eredménynek klinikai jelentősége is van, mivel már ma is létezik a kereskedelmi forgalomban egy szer, a rovelizumab, amely a CD18-hoz kötődve gátolja a CD18-integrin komplexek, köztük a CD18-CD11b aktivitását. A rovelizumab biztonságossági profilja kiváló, azonban azok ellen a generalizált gyulladásos betegségek (pl. sclerosis multiplex) ellen, amelyekben kipróbálták, igen csekély hatása volt. Ez nem is csoda, hiszen testszerte óriási mennyiségű CD18-CD11b-pozitív makrofág van, és a gyógyszerhatás eléréséhez valószínűleg mindet semlegesíteni kellene. Ahn és munkatársai azért tudtak a tumorok esetében sikert elérni, mert csak a tumorban felgyűlt makrofágokat célozták meg a kezeléssel, és elvileg ez emberben is megvalósítható.
(Joseph E. Qualls, Peter J. Murray: Stopping macrophages wounds tumors. Nature Medicine, 2010, 16:863-864.)
A makrofágok számos gyulladásos és immunszuppressziós mechanizmus révén befolyásolják a tumorfejlődést, ami lehetőséget teremt arra, hogy a hagyományos stratégiák – besugárzás, kemoterápia – mellett más módon is küzdjünk a tumor ellen.
Ahn és munkatársai nemrég igazolták, hogy a makrofágok döntő szerepet játszanak a daganatok besugárzás utáni helyreállásában. Modelljükben a besugárzás után antitestet alkalmaztak egy, a legtöbb makrofág által expresszált sejtfelszíni integrin, a CD11b ellen, és ezzel megakadályozták a makrofágok migrációját a daganat maradványába. A kezeléssel nagyon jó eredményt értek el: a tumor nem növekedett ismét a besugárzást követően. Az ilyen kezelés hasznos adjuváns terápia lehet szolid tumorok esetében.
A szolid tumorokat nagy számban elárasztó makrofágokat tumor-assszociált makrofágoknak
(TAM) nevezik. Számos kutatás keres választ olyan kérdésekre, hogy mi váltja ki a makrofágok felszaporodását a daganatokban, milyen funkciót töltenek be a be a TAM-ok és miként gátolhatók a TAM-ok tumortámogató mechanizmusai. Jelenlegi tudásunk szerint a makrofágok segítik a daganatok növekedését, vagyis káros hatásúak a gazdaszervezetre nézve, Ezt klinikai bizonyítékok is alátámasztják: a makrofágok inváziója rossz kimenetellel jár, főként az emlődaganatok esetében és az emlőrákok egérmodelljeiben.
Más nézőpontból viszont a makrofágok éppen azt teszik, ami elvárható tőlük: a „sérült” (tumorba hatolnak, és az immunszuppresszív környezetben végrehajtják javító-helyreállító funkciójukat. Hasonlóan viselkednek, mint például steril gyulladás (pl. csonttörés, ínsérülés, belső szervi sérülés) esetén: a sérülés helyére gyűlnek, eltávolítják az elpusztult sejteket és a szövettörmeléket, és végül a szövetsérülés begyógyul. Kulcsfontosságú, hogy a szövet, illetve a tumor helyreállítása immunszuppresszív környezetben történjen, mivel igen nagy az esélye a sérült szövet vagy a tumor antigénjei elleni autoimmunitás kialakulásának. A TAM-ok egyik legfontosabb funkciója tehát valószínűleg az immunszuppresszió kialakítása. Ahn és munkatársai egy másik vizsgálata szerint a TAM-ok másik fontos szerepe a gyógyulás egyik részfolyamatának, az érképződésnek a serkentése – revaszkularizáció hiányában a tumor nem indulhatna növekedésnek. Ezt a funkciót az teszi lehetővé, hogy a makrofágok vaszkuláris endoteliális növekedési faktort termelnek, és elősegítik az érhálózatok kialakulását is.
A CD11b integrin a legtöbb makrofág és neutrofil leukocita felszínén megtalálható. Ennek – monoklonális antitesttel történő – gátlásával érte el Ahn kutatócsoportja a makrofágok tumorsegítő aktivitásának megszüntetését. Az eredménynek klinikai jelentősége is van, mivel már ma is létezik a kereskedelmi forgalomban egy szer, a rovelizumab, amely a CD18-hoz kötődve gátolja a CD18-integrin komplexek, köztük a CD18-CD11b aktivitását. A rovelizumab biztonságossági profilja kiváló, azonban azok ellen a generalizált gyulladásos betegségek (pl. sclerosis multiplex) ellen, amelyekben kipróbálták, igen csekély hatása volt. Ez nem is csoda, hiszen testszerte óriási mennyiségű CD18-CD11b-pozitív makrofág van, és a gyógyszerhatás eléréséhez valószínűleg mindet semlegesíteni kellene. Ahn és munkatársai azért tudtak a tumorok esetében sikert elérni, mert csak a tumorban felgyűlt makrofágokat célozták meg a kezeléssel, és elvileg ez emberben is megvalósítható.