A gyógyszergyárak harca saját gyógyszerük ellen
A National Health Service (NHS), a nagy-britanniai országos társadalombiztosító szervezet egy lépéssel közelebb jutott ahhoz, hogy befogadjon egy olcsó gyógyszert, amely a vakságot leggyakrabban okozó betegségre hat – annak ellenére, hogy a gyógyszergyárak ezt lehetetlenné akarják tenni.
A National Institute for Health and Clinical Excellence (NICE), az a szervezet, amely eldönti, hogy milyen gyógyszereket lehet az NHS támogatásával felírni, úgy döntött, hogy hivatalosan engedélyezni fogja a bevacizumab hatóanyag-tartalmú olcsó gyógyszert, amelyet már széles körben használnak off-label az időskori makuladegeneráció (AMD) nedves formájának megelőzésére. Teszi ezt annak ellenére, hogy a gyógyszert gyártó és forgalmazó cégek nem hajlandók kérni a gyógyszer törzskönyvezését ebben az indikációban. Ennek oka, hogy már gyártanak egy olyan, a bevacizumabhoz kémiailag és klinikailag nagyon hasonló szert, a ranibizumabot, amelyet már törzskönyveztek szemészeti alkalmazásra, és amely jóval drágább, mint a bevacizumab.
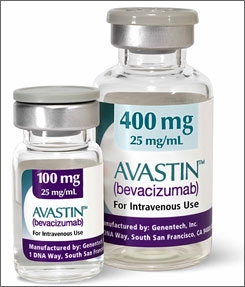
A bevacizumabot bélrák kezelésére törzskönyvezték, de amerikai szemészek felfedezték, hogy – olyan kicsiny dózisokra osztva, amelyek injektálhatók a szembe – megállítja, sőt, gyakran visszafordítja az AMD folyamatát, ami a vakság leggyakoribb oka. A szemészek ma már szerte a világon alkalmazzák ezt a szert, mivel egy ampullányiból nagyon sok szemészeti adag telik ki, és ezért viszonylag olcsó.
A gyártó küzdelme saját gyógyszere ellen
A gyógyszer gyártója, a Genentech, és a gyógyszert Nagy-Britanniában forgalmazó Roche azonban küzd a bevacizumab ilyetén felhasználása ellen. A Genentech gyártja ugyanis a jóval drágább, ranibizumab hatóanyagú, szemészeti alkalmazásra már törzskönyvezett és az NHS által befogadott gyógyszert is. Míg egy szemészeti dózis a bevacizumabból 50 fontba kerül, a ranibizumabból mintegy 750-be, azaz 15-ször annyiba.
A kezelés havi egy injekcióból áll három hónapon át, vagy ha a beteg látása tovább romlik, akár tovább is. Mivel a ranibizumab árát a NICE magasnak tartja, a Novartis, amely a szer nagy-britanniai forgalmazója, vállalta, hogy kifizeti azoknak a betegeknek a további gyógyszerköltségét, akik már legalább 14 injekciót kaptak. De mivel Nagy-Britanniában évente 20 000 betegben diagnosztizálják a nedves AMD-t, a költség még így is nagyon sokra rúg. Ezért a NICE, amely egyébként nem szokott engedélyezni az adott indikációban nem törzskönyvezett gyógyszereket, úgy döntött, hogy a bevacizumabbal kivételt tesz, és most már csak az Egészségügyi Minisztérium jóváhagyását várják.
A vakok országos szövetsége is tiltakozik
A döntést a gyógyszergyárak rosszallják. A Roche (amely megvette a Genentechet) azt nyilatkozta, hogy szervezeti megfontolások miatt nem törzskönyveztette a bevacizumabot szemészeti alkalmazásra, és a jövőben sincs ilyen szándéka. A gyógyszergyárak figyelmeztették a NICE-t, hogy a szer oftalmológiai alkalmazása biztonságosságának monitorozása az ő részvételük nélkül nem valósítható meg – és ők nem fognak segíteni ebben. Ezért a gyógyszer engedélyezését helytelen lépésnek tartanák.
A vakok országos szövetsége, amely támogatást kap a gyógyszergyáraktól, szintén ellenzi a bevacizumab engedélyezését, nagyjából a gyógyszercégek biztonságosságra vonatkozó érveit visszhangozva.
Mindezek ellenére, mivel az NHS pénzhiánnyal küszködik, az alapellátók szövetségei már a lábukkal szavaztak. A Stockport szövetség például részletesen ismerteti a betegekkel a bevacizumabra és a ranibizumabra vonatkozó információkat, és a döntést a betegekre bízza; nagy többségük a bevacizumabot választja. A helyzet a többi alapellátó szövetségben is hasonló.
Újabb embrionális őssejt kipróbálást engedélyezett az FDAAz Advanced Cell Technology elnevezésű amerikai biotechnológiai cég hétfői bejelentése szerint az Egyesült Államok gyógyszerügyi hatósága, az FDA engedélyezte, hogy megkezdje a második olyan klinikai próbát, amelyben humán embrionális őssejteket használnak bizonyos típusú látásvesztés kezelésére. A mostani kipróbálásban - melyben idősebb emberek vesznek majd részt - a módszer biztonságosságát tesztelik. A klinikai tesztbe száraz időskori makuladegenerációban (AMD) szenvedő betegeket vonnak be. Az időskori látásvesztés gyakori oka az ideghártya éleslátásáért felelős területének elfajulása. Mint Robert Lanza, a vállalat tudományos igazgatója közleményében kiemelte, a népesség öregedésével egyre több embert érint az időskori makuladegeneráció, amelynek száraz formája az 55 év fölöttieknél a látásvesztés vezető oka. A betegséggel érintettek száma a következő húsz évben várhatóan megduplázódik. Becslések szerint 10-15 millió amerikait is érinthet az AMD. |