A vese a vérnyomás szabályozója és a hipertóniás szövődmények fontos szerve
A magas vérnyomás és a krónikus vesebetegség (CKD) is előfordulásigyakoriságuk alapján népbetegségnek tekinthetők, a két betegség közötti szoros kapcsolat régóta jól ismert. Ezért a krónikus vesebetegek hipertóniájának kezelése kiemelt jelentőségű. A hipertónia az egyik legfontosabb kockázati tényezője – a kardiovaszkuláris betegségek mellett – a vesefunkció további romlásának és a későbbi szövődmények kialakulásának.
A 2024-ben megjelent Európai Kardiológustársaság- (ESC), Európai Hipertóniatársaság- (ESH) illetve a szintén 2024-es KDIGO (Krónikus Vesebetegségek Felismerését és Kimenetelét Javító) ajánlás egy újfajta holisztikus szemlélet kialakítását javasolja a hipertóniás, illetve CKD-s hipertóniás betegek esetén egyaránt.Az új ajánlásokban a hipertóniás és CKD-s betegek célvérnyomása nem változott a korábbiakhoz képest, jelenleg is a kombinációban kezdett, lépcsőzetesen felépített vérnyomáscsökkentő kezelés javasolt. A renin-angiotenzin-aldoszteron rendszer gátlásának előnyei továbbra is fontos szerepet játszanak mind a CKD-s,mind a nem CKD-s hipertóniás betegek kezelésében. A kiegészítő – elsődlegesen nem vérnyomáscsökkentő – terápia alkalmazásának (pl. nátrium-glükóz kotranszporter-2-receptor-gátlók[SGLT2i], nemszteroid típusú mineralokortikoid receptoragonisták[MRA], mint a finerenone,glukagonszerű peptid-1-receptor-agonisták[GLP1-RA]) kiemelése egyre nagyobb hangsúlyt kap a hipertónia kezelésére összeállított legújabb irányelvekben is. Annálnagyobb egészségnyereséget tudunk elérni betegeink számára,minél korábban kezdjükel a hipertónia és a CKD kezelését, ezt támasztják alá az egyre növekvő tudományos bizonyítékok is.
Az elmúlt 12 hónapban 3 új szakmai ajánlás is megújult. Az Európai Kardiológustársaság (ESC) és az Európai Hipertóniatársaság (ESH) hipertóniaajánlása, valamint a KDIGO (Kidney Disease Improving Global Outcomes) a krónikus vesebetegségek felismeréséről és kezeléséről is új szakmai irányelvet adott ki. Mindhárom ajánlásban egy teljesen új, holisztikus szemlélete figyelhető meg a hipertónia és a krónikus vesebetegség felismerésének és kezelésének.
A krónikus vesebetegséget ma úgy határozzuk meg, hogy a három hónapon túl tartósan fennálló beszűkült vesefunkció, tehát az alacsony becsült glomeruláris filtrációs ráta (bGFR 3 mg/mmol] arány, vagy egyéb laboratóriumi vagy képalkotó-kritérium alapján) (1). A CKD és fehérjevizelés stádiumbeosztása az 1. és a 2. táblázatban látható (2).
- táblázat: A CKD stádiumainak beosztása
|
GFR-stádium |
GFR (ml/perc/1,73 m²/*/) |
Meghatározás |
|
G1 |
≥90 |
normális vagy fokozott veseműködés |
|
G2 |
60–89 |
enyhén csökkent veseműködés |
|
G3a |
45–59 |
enyhe-mérsékelt veseműködés-csökkenés |
|
G3b |
30–44 |
mérsékelt-súlyos veseműködés-csökkenés |
|
G4 |
15–29 |
súlyosan csökkent veseműködés |
|
G5 |
<15 |
végstádiumú vesebetegség |
2. táblázat: A fehérjevizelés stádiumainak beosztása
|
Albumin-, proteinuriastádium |
Meghatározás |
Albuminuria (mg/nap) |
Proteinuria (mg/nap) |
ACR (mg/mmol) |
TPCR (mg/mmol) |
|
A1, P1 |
normális/enyhén emelkedett |
<30 |
<150 |
<3 |
<15 |
|
A2, P2 |
mérsékelten emelkedett |
30–300 |
150–500 |
3–30 |
15–50 |
|
A3, P3 |
jelentősen emelkedett |
>300 |
501–3500 |
>30 |
51–350 |
|
A3n, P3n |
nefrotikus |
|
>3500 |
|
>350 |
ACR: albumin/kreatitin ráta; TPCR: összfehérje/kreatinin ráta
Számos korábbi nemzetközi tanulmány és irodalmi adat igazolta, hogy a hipertónia a halálozás egyik legfontosabb, befolyásolható kockázati tényezőjének tekinthető világszerte (3). Az Egészségügyi Világszervezet (WHO) 2023 szeptemberében adott ki jelentést a magas vérnyomás globális hatásairól(4). A jelentésben foglaltak szerint a magas vérnyomással élők száma 1990 és 2019 között megduplázódott a világon, 650 millióról 1,3 milliárdra nőtt. Világszerte a magas vérnyomásban szenvedő emberek közel fele nem tud a betegségéről, és körülbelül minden ötödiket nem kezelnek megfelelően. Hazánkban a 30–79 éves lakosság körében a férfiak 56, a nők 41%-a szenved magasvérnyomás-betegségben(4).
Világszerte hozzávetőleg 850 millió ember szenved CKD-ben, több mint 80%-uk hipertóniás, és a prevalencia 15 éven belül várhatóan 1,56 milliárdra emelkedik (5). Egy közelmúltban történt vizsgálat igazolta, hogy Magyarországon az idült vesebetegség előfordulási gyakorisága 15-17% körül van. A jó hír az, hogy mind a magas vérnyomás, mindaz idült vesebetegség szövődményeimegelőzhetőek, és korán felismerve kezelhetőek is. Azonban minél tovább áll fenn diagnosztizálatlan és/vagy nem megfelelően kezelt magas vérnyomás és idült vesebetegség, annál rosszabbak lesznek a betegek hosszú távú kilátásai és életminősége(6).
Ismert, hogy avese és a magas vérnyomás szoros kapcsolatban áll egymással, a vese erőteljes szabályozója a vérnyomásnak (BP) – számos szabályozórendszeren keresztül (talán az egyik legfontosabb a renin-angiotenzin-aldoszteronrendszer=RAAS) – ésegyben a hipertónia okozta célszervkárosodás fontos szerve.Vagyisavesefunkció romlása hozzájárul a vérnyomás kezdeti emelkedéséhez, míg amagas vérnyomás elősegíti a balkamra-hipertrófia és a krónikus vesebetegség (CKD) kialakulását és progresszióját.Erre utal, hogy a hipertónia a második leggyakoribb tényező a végstádiumúvesebetegségkialakulásában a diabetes mellitus után, amely szintén nagyon gyakran társul hipertóniával(7).Közös rizikótényezők (mint az obezitás, diabétesz, diszlipidémia, dohányzás, öregedés) szerepet játszanak mind a hipertónia, mind az idült vesebetegség kialakulásban. A hipertónia fontos tényezője az erekben kialakuló ateroszklerózisnak és a veseelváltozásoknak (glomeruloszklerózis, tubuláris atrófia és interszticiális fibrózis). Mindezen folyamatok tovább emelik a betegek vérnyomását, és rontják a vesefunkciót, ezzel „circulus vitiosust” okozva (1. ábra).
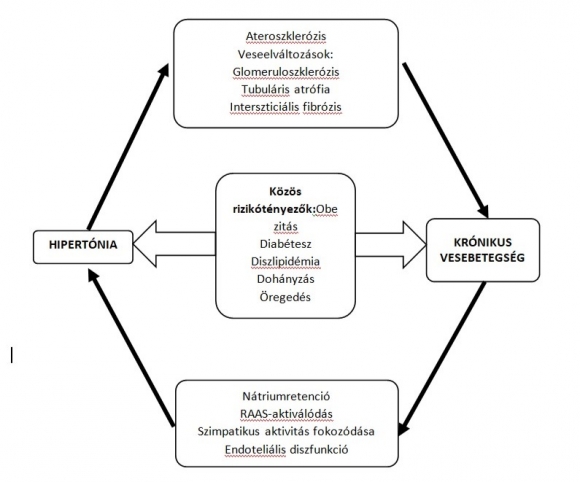
A hipertónia ésa CKD együttesen elősegítik a szív- és érrendszeri (CV) betegségek kialakulását és progresszióját (8), ami arra hívja fel a figyelmet, hogy orvosként apácienst globálisan szemlélve, az összes kockázatitényezőjét befolyásolni szükséges: csökkentsük a magas vérnyomást, lassítsuk a GFR-vesztést, mérsékeljük az albuminuriát és korrigáljuk a szív- és vesebetegségekkel kapcsolatos egyéb kockázati tényezőket, mint a diszlipidémia, diabetes mellitus, elhízás és dohányzás. Mindez egy új szemlélet létrejöttét alapozta meg, holisztikusan szemlélve a kardio-reno-metabolikus egészség meglétét vagy hiányát vizsgálva (9).
Az emelkedett vérnyomás és a hipertónia által hátrányosan érintett szervek közé tartozik a szív, az agy, a vesék, a szemek és az erek (makrokeringés és mikrokeringés az alacsony ellenállású szervekben, mint pl. az agy vagy a vese), amelyek strukturális és funkcionális változásokon mennek keresztül. Bár a vérnyomáson kívül más tényezők is hozzájárulhatnak ezekhez a változásokhoz (azaz diszlipidémia, hiperglikémia), a „hipertónia által közvetített szervkárosodás” (HMOD) kifejezést használjuk a szubklinikus, a hipertónia okozta szövődmények leírására, amelyek nagy kockázatot jelezhetnek a későbbiekben a klinikai kimenetel vonatkozásában. A HMOD profilja eltérő lehet a férfiak és a nők esetében; például a bal kamrai hipertrófia (LVH) és a bal pitvari dilatáció nőknél gyakoribb (10–14).Kezelés hiányában a HMOD tünetmentesről tünetessé fejlődhet, ami végül CV-események kialakulását eredményezheti (15).
A hipertónia prevalenciája az elmúlt évtizedekben jelentősen emelkedett, különösen a gyermekek és fiatalok körében, az elhízás, a magas étrendi nátriumbevitel, a mozgásszegény életmód, a gyakoribbá váló koraszülöttség (pl. alacsony nefronszám) és a társadalmi-gazdasági tényezők miatt. Ezért a gyermekkori magas vérnyomás felismerése fontos,mert ha nem kezelik, hozzájárul a szubklinikus szív-érrendszeri betegségekkorai kialakulásához, és a korábban kialakuló veseműködési zavar jelentős kockázati tényezővé vállhat (16). A gyermek- és serdülőkori elhízás, a cukorbetegség és a magas vérnyomás megfelelő kezelése szükséges a kialakult kardiorenális betegségkockázat csökkentéséhez és a kialakulás megelőzéséhez.
Az irányelvek
Magas vérnyomás esetén (RR>140/90 Hgmm) csökkentenünk kell a vérnyomást, de az elérendő célvérnyomásértékekben az ajánlások kissé eltérőek (3. és 4. táblázat).Ahipertónia kezelésének irányelvei azt a célt tűzték ki, hogy a vérnyomás célértéke<130/80 Hgmm alatt legyen, amennyibenmagas vérnyomás kíséri a CKD-t.A KDIGO (krónikus vesebetegség felismerésére és a kimenetel javítására) vonatkozó irányelv a 120/80 Hgmm-t határozza meg optimális célértékként (5).A vérnyomásértékek kapcsán megfigyelték, hogy már a kóros érték felé közelítve növekednek a szövődmények, ezért bevezették az optimális/normális/magasnormális kategóriákat.
3. táblázat: A vérnyomásértékek újabb osztályozása (a klinikai jelentőségük fokozott figyelembevételével)
|
ESH 2023 ajánlás Vérnyomás kategóriák |
Szisztolés vérnyomás (Hgmm) |
Rendelői vérnyomás (Hgmm) |
ESC 2024 ajánlás Vérnyomás katagóriák |
|
Optimális |
<120/80 |
< 120/70 |
Nem emelkedett vérnyomás |
|
Normális |
120–129/80–84 |
120/70 – < 140/90 |
Emelkedett vérnyomás |
|
Magas normális |
130–139/85–89 |
||
|
1. fokú hipertónia |
140–159/90–99 |
≥ 140/90 |
Hipertónia |
|
2. fokú hipertónia |
160–179/100–109 |
||
|
3. fokú hipertónia |
≥180/110 |
4. táblázat: Célvérnyomás CKD-s hipertóniás betegeknél az ajánlások alapján 2024-ben
|
Ajánlás |
ESH 2024 |
ESC 2024 |
KDIGO 2024 |
|
Célvérnyomás (Hgmm) |
120–140/70–80
|
120–130/70–80 |
<120/80 |
A CKD-ban az albuminuria kapcsán hasonló jelenség figyelhető meg. CKD esetén a magas normális albuminuria meghatározásához használt küszöbérték 1 mg/mmolalbumin/kreatinin, míg az átlagos magas albuminuria esetében (önellátó kritérium a CKD diagnosztizálásához, ha 3 hónapnál tovább fennáll) 3 mg/mmolalbumin/kreatinin, de az1 és 3 mg/mmol közötti értékek is kezelést igényelnek az albuminuria progressziójának és az ebből eredő szív- és vesebetegségek kockázatnövekedésének megelőzése érdekében, azonban az ajánlásokban ez a megközelítés nem szerepel(17–18).
Ezenkívül a vérnyomás-emelkedés és a vesekárosodás kialakulásának korai megelőzése megakadályozhatja a kis erek szubendoteliális károsodását és az artériás merevség kialakulását, ezek a kardiorenális betegség két kulcsfontosságú tényezője, amelyek gyakran megelőzik a vérnyomás emelkedését (19). Ezért a javasoltnál korábbi időszakaszokban van szükség intervenciós beavatkozásokra és ezzel kapcsolatos szakmai irányelvekkialakítására.
Ahipertónia, a CKD progressziójának és a szív- és érrendszeri betegségeknek a kezelése kulcsfontosságú terápiás cél, és gyakori optimalizálást igényel. Az életmód változtatása mellett, a vérnyomáscsökkentő gyógyszeres terápia alkalmazása során a legtöbb esetben szükséges kettőnél több gyógyszer alkalmazása a célérték eléréséhez, amitúlnyomórészt fix gyógyszer-kombinációk formájában történik. A renin-angiotenzin-aldoszetron rendszerre (RAAS) ható gyógyszerek alkalmazása elsődleges ezeknél a betegeknél, mivel egyidejű vese-, szív- és érrendszeri védelmet nyújtanak a megfelelő vérnyomás-szabályozáson túl. A RAS-blokkolók, mineralokortikoid receptor antagonisták (MRA) és nátrium-glükóz kotranszporter-2-gátlók (SGLT2i), cukorbeteg vagy elhízott betegeknél glukagonszerű peptid-1-receptor-agonisták (GLP-1-RA), valamint a diszlipidémia kezelésére szolgáló gyógyszerek is a legtöbb betegnél szükségesek lehetnek.
Európai Kardiológustársaság (ESC) 2024-es ajánlása
Az új, 2024-es ESC-ajánlás új megközelítést és irányelveket tartalmaz, kiemelve az egyéni kockázatértékelés, az életmódbeli beavatkozások és a gyógyszeres terápiák szerepét (20, 21). Új vérnyomás-kategóriák és -célértékek bevezetése szerepel a javaslatukban: a 2024-es ESC-irányelvek szerint a „nem emelkedett vérnyomás” (korábbi WHO-, illetve ESH-ajánlásban optimálisnak nevezett vérnyomás) <120/70 Hgmm. Bevezették az „emelkedett vérnyomás” kategóriát, amelyhez a szisztolés vérnyomást 120–139 Hgmm, a diasztolés vérnyomást 70–89 Hgmm közötti tartományban határozták meg(a korábbi normális és magasnormális tartományok leírására). A „magas vérnyomás” definíciója továbbra is ≥140/90 Hgmm maradt. A „magas vérnyomás” kategóriába tartozó betegeket javasolt kezelni, míg az új, „emelkedett vérnyomás” kategóriába tartozó betegeknél tanácsos kardiovaszkuláris kockázati besorolást végezni, mielőtt döntés születik a kezelésről. Az elkövetkező évek orvosi gyakorlata fogja bizonyítani, hogy ez mennyire lesz használható//(3. táblázat)//. Az új célérték a vérnyomáscsökkentő gyógyszerekkel kezelt felnőttek számára a szisztolés vérnyomás esetén 120–129 Hgmm, feltéve, hogy a kezelés jól tolerálható, és nincs kockázata a túlságosan alacsony vérnyomásnak//(4. táblázat)//.
A legtöbb emelkedett vérnyomásban és cukorbetegségben szenvedő felnőttnél maximum 3 hónapos életmódbeli beavatkozás után javasolt a vérnyomás gyógyszeres kezeléssel történő csökkentése, akiknél az igazolt rendelői vérnyomás magasabb, mint ≥130/80 Hgmm, a szív- és érrendszeri betegségek kockázatának csökkentése érdekében (22, 23).
A vérnyomáscsökkentő gyógyszeres kezelés a prediabéteszes vagy elhízott betegek számára akkor javasolt, ha a rendelői vérnyomás igazoltan ≥140/90 Hgmm, vagy ha a rendelői vérnyomás 130–139/80–89 Hgmm közötti, és a betegnél CVD 10 éves kockázata ≥10% áll fenn, vagy a maximum 3 hónapos életmód-terápia ellenére is fennáll a magas kockázatú állapot (22). Ezen irányelvek alkalmazásában a közepesen súlyos vagy súlyos CKD-ben és emelkedett vérnyomásban szenvedő felnőttek kellően magas kockázatnak vannak kitéve ahhoz, hogy megfontoljuk a vérnyomáscsökkentő gyógyszeres terápia alkalmazását. A KDIGO szerint a CKD-stádiumokat használjuk kockázat meghatározására. Közepestől súlyoskockázatig terjedő személyek azok, akik bGFR-értéke
Az új ajánlás olyan kutatási eredményekre támaszkodik, amelyek bizonyítják, hogy az alacsonyabb vérnyomás kevesebb kardiovaszkuláris eseményt eredményez. Az irányelvek hangsúlyozzák az életmódbeli változtatások szerepét, például a napi nátrium-klorid-bevitel 5 g alá történő csökkentését. Valamint a heti legalább 150 perc közepes intenzitású aerob testmozgást vagy 75 perc erőteljes intenzitású mozgást.Ezek a változtatások bizonyítottan csökkenthetik a vérnyomást és a kardiovaszkuláris események kockázatát. A gyógyszeres kezelések terén az irányelvek azt javasolják, hogy a vérnyomáscsökkentő gyógyszereket a beteg a számára legkényelmesebb időpontban vegye be, mivel ez javítja a terápiahűséget. Emellett javasolt, hogy a gyógyszeres kezelést élethosszig folytassák, még 85 év felett is, ha jól tolerálható.
A vérnyomáscsökkentőkezelést egyénileg kell megtervezni, előnyben részesítve a hosszú hatású kalciumcsatorna-blokkolókat vagy RAS-gátlókat, amennyiben a terápia jól tolerálható. A vesedenerváció először szerepel az irányelvekben, mint a rezisztens hipertónia kezelésében alkalmazott eljárás, amely a veseartériák szimpatikus idegeinek megszakításával csökkenti a vérnyomást. A vesedenerváció elsősorban olyan betegeknél lehet indokolt, akiknél a vérnyomás a rezisztens hipertónia miatt nem kontrollálható, és akiknél magas a kardiovaszkuláris események kockázata. Nem javasolt erősen károsodott vesefunkciójú pácienseknek vagy magas vérnyomás másodlagos okai miatt szenvedőknek. Az új irányelvek kiemelik a betegközpontú megközelítést, amely magában foglalja a páciensek bevonását a döntéshozatalba, valamint a motivációs interjúk és az otthoni vérnyomásmérés alkalmazását a kezelés eredményességének javítása érdekében. Ezek az ajánlások segítenek a napi gyakorlatban alkalmazott kezelési stratégiák javításában, különös figyelmet fordítva az egyéni kockázatokra és a betegek preferenciáira.
Legfontosabb ajánlások CKD és hipertónia esetén az ESC-ajánlásból:
Cukorbetegeknél vagy nem cukorbetegeknél, közepesen súlyos vagy súlyos CKD és igazolt ≥130/80 Hgmm vérnyomás esetén, életmód-optimalizálás és vérnyomáscsökkentés, gyógyszeres kezelés javasolt a szív- és érrendszeri betegségek kockázatának csökkentésére, feltéve, hogy az ilyen kezelést jól tolerálják a betegek (24, 25) (1A ajánlás).
Súlyos CKD-ban (bGFR
Hipertóniás betegeknél, akiknél CKD és bGFR >20 ml/perc/1,73 m²/*/, az SGLT-2-inhibitorok javasoltak (28, 29) (1A ajánlás).
Az ACE-gátlók vagy az ARB-k hatékonyabban csökkentik az albuminuriát, mint más vérnyomáscsökkentő szerek, és a kezelési stratégia részének kell tekinteni a magas vérnyomásos és mikroalbuminuriás vagy proteinuriás betegek esetén (30–32) (2a B).
Európai Hipertóniatársaság (ESH) 2024 (Practice Guideline) Gyakorlati irányelvek Útmutató (33)
Az ESH könnyen memorizálható (MASTER) mozaik szóval világítja meg a hipertóniás betegek felismerését és kezelését.Ennek a megközelítésnek négy alappillére van: az első a mérjük a beteg vérnyomását és diagnosztizáljunk (Measure). A második, értékeljük a beteget (Assess),vagyis becsüljük meg a beteg rizikóját. A harmadik, válasszunk kezelést a beteg számára (Select Therapy),és a negyedik, értékeljük a beteg terápiás válaszát (Evaluate Response) 3 lépcsőben a terápiakezdéstől vagy -módosítástól 3 hónap, 3 hónap és egy év között és egy év elteltével.
ESH 2023 és 2024 ajánlása alapján
A hipertóniás krónikus vesebetegek kezelésében számos kérdésre még nem tudjuk apontos választ. Utalunk itt a célvérnyomásérték, illetve a gyógyszeres kombinációkkal kapcsolatos adatok hiányára. Fontos azonban, hogy kiemeljük azokat a követendő irányelveket, amelyeket több kontrollált, randomizált vizsgálatban is igazoltak, ezért tényként fogadhatjuk el.
Legmagasabb szintű (I/A) bizonyítékok a hipertóniás CKD-ban szenvedő betegek kezelésében
1. A vérnyomást a CKD minden stádiumában ellenőrizni kell, mivel a hipertónia a legfontosabb kockázati tényező a végállapotú veseelégtelenség kialakulásában.
2. Mind diabéteszes, mind nem diabéteszes hipertóniás CKD-betegben a vérnyomáscsökkentő kezelés lassítja a vesefunkció-romlás ütemét, a végállapotú veseelégtelenség kialakulásának és a CV-esemény lehetőségét.
3. Minden CKD-s betegben elsődleges cél a rendelői vérnyomás <140/90 Hgmm elérése.
4. Mérsékelt (UACR 3–30 mg/mmol) vagy súlyos (UACR > 30 mg/mmol) proteinuriás CKD-ban az ACE-gátló vagy ARB dózisát a maximálisan tolerálható dózisig kell feltitrálni.
5. SGLT2-gátló kezelés indítása javasolt mind diabéteszes, mind nem diabéteszes CKD-s betegeknek, ha a bGFR > 20 ml/min/1,73 m²/*/.
6. Nemszteroid hatású MRA – finerenone javasolt 2-es típusú diabéteszes, albuminuriás, CKD-betegeknek, ha eGFR > 25 ml/min/1,73 m²/*/.
KDIGO 2024 ajánlás
A KDIGO ajánlásöt fejezetben foglalja össze az új irányelveit: a CKD értékelése,kockázatértékelés CKD-s betegeknél, a CKD progressziójának késleltetése és a szövődmények kezelése, az orvosi menedzsment és gyógyszerelés kezelés CKD-ban, optimális gondozási modellek(34).
A CKD felismerése
Az első fejezet rávilágít a CKD kimutatásának fontosságára a magas kockázatú populációkban, mert a CKD gyakran „néma”,és a betegek a korai szakaszban tünetmentesek lehetnek. Aszűrési algoritmus a CKD diagnosztizálására felnőtteknél kiemeli az alapvető vizsgálati módszerek alkalmazását, majd részletezi az alapos értékelés fontosságát: a bGFR és a vizelet albumin-kreatinin arány (UACR) eltérésénekoka és pontos értékelése, majd a páciensek megfelelő besorolása.
CKD rendszeres vér- és vizeletvizsgálattal követhető, az egyén kockázata alapján mérhető, mindkettő útmutatást ad a páciensek követése során az időbeli változásokról, amelyet a klinikusoknakkell értelmezniük.
Az ajánlás a prevenciós stratégiák fontosságát hangsúlyozza: ellentétben azonban a cukorbetegséggel vagy a szív- és érrendszeri betegségekkel, a vesebetegségekre vagy a magas vérnyomásra vonatkozó irányelvek csak ritkán hangsúlyozzák a megelőzési stratégiákat. Ebből következően a magas vérnyomás és a CKD korai megelőzési stratégiái gyakran nem kapnak megfelelő hangsúlyt. Az emelkedett vérnyomás és a CKD kialakulásának korai kockázati tényezőinek jellemzése és kezelése kulcsfontosságú az egészségre káros következményeik csökkentése érdekében. A kockázati tényezők csökkentése érdekében javasolt és elég csak négy dolgot tenni. Ezek mindegyike önállóan is hozzájárul a jó egészségi állapothoz, de a leghatékonyabb mégis az, ha egyszerre valósítjuk meg:
1. egészséges táplálkozás, beleértve a sószegény étrendet és így az egészséges testsúly fenntartását,
2. túlzott alkoholfogyasztás kerülése,
3. dohányzás mellőzése, illetve dohányzásról történő leszokás,
4. rendszeres testmozgás.
A KDIGO 2024 ajánlás kiemelten foglalkozik az utóbbi években bebizonyított vesevédő hatású gyógyszerekkel a már ismert és elfogadott RAS-gátló kezelés mellett. Ezek szintén megemlítésre kerülnek az ESH-, ESC-ajánlásokban is, de mivel a vérnyomáscsökkentő hatásuk kevésbé markáns, tárgyalásuk is rövidebb. ACKD terápiájára vonatkozó része az ajánlásnak 4 gyógyszercsoportot említ a kezelést illetően, ezek a RAS-gátlók, SGLT-2-gátlók, MRA-k és GLP-1-RA-k.
Renin-angiotenzin rendszer gátlók:
Az irányelvek javasolják aRAS-gátló (angiotenzinkonvertáló-enzim-gátló [ACEi], ill. angiotenzin-II-receptor-blokkoló [ARB]) adását CKD-ban és súlyosan megnövekedett albuminuria esetén (G1–G4, A3), cukorbetegség nélkül (1B).
RAS-gátlók (ACEi vagy ARB) megkezdését CKD-ban és mérsékelten fokozott albuminuria (G1-G4, A2) esetén cukorbetegség nélkül (2C).
RAS-gátló (ACEi vagy ARB) kezelés megkezdését javasolják krónikus vesebetegségben szenvedő és közepes vagy súlyos albuminuria esetén (G1–G4, A2 és A3) cukorbetegeknek (1B).
Az irányelvek az ACEi-, ARB- és a direktrenin-gátló (DRI) terápia kombinációjának kerülését javasolják olyan betegeknél,akik CKD-ben szenvednek, cukorbetegséggel vagy anélkül (1B).RAS-gátlót (ACEi vagy ARB) a leírt előnyök elérése érdekében a legnagyobb megengedett/tolerálható dózissal kell alkalmazni,mert a bizonyított előnyöket ezekkel az dózisokkal végzett vizsgálatokban érték el.A vérnyomás, a szérumkreatinin és a szérumkálium változásait a kezelés megkezdését vagy a dózis növelését követő 2–4 héten belül ellenőrizni kell.A RAS-gátlók használatával összefüggő hiperkalémia kialakulása gyakran a szérumkáliumszintet csökkentő beavatkozásokkal kezelhető inkább, mint az adag csökkentésével vagy a RAS-gátló leállításával.ACEi- vagy ARB-terápia folytatása javasolt, kivéve, ha a szérum kreatininszintje 30%-nál nagyobb mértékben emelkedik a kezelés megkezdését követő 4 héten belül. Mérlegelni kell az adag csökkentését, vagy az ACEi, vagy az ARB megszakítását tüneti hipotenzió vagy az orvosi kezelés ellenére fennálló hiperkalémia esetén,vagy az urémiás tünetek csökkentése érdekében veseelégtelenség kezelése során (bGFR
Nátrium-glükóz kotranszporter-2 inhibitorok (SGLT2i):
2-es típusú cukorbetegségben (T2D) és CKD-ban a ≥20 ml/perc/1,73 m²/*/bGFR-értékkel rendelkező betegek SGLT2i-kezelést javasolnak (1A).
Az SGLT2i elindítása után észszerű folytatni az SGLT2i-t, még akkor is, ha az bGFR 20 ml/perc/1,73 m²/*/ alá esik, hacsak nem tolerálható, vagy vesepótló kezelést kezdenek.Észszerű lehet az SGLT2i-kezelés megszakítása hosszan tartó koplalás, műtét vagy kritikus egészségügyi betegség idején (amikor nagyobb a ketózis kockázata).CKD-ban szenvedő felnőttek esetén SGLT2i-vel történő kezelést javasolnak a következők esetén (1A):bGFR ≥20 ml/perc/1,73 m²/*/ (empagliflozin esetén), illetve bGFR≥25 ml/perc/1,73 m²/*/ (dapagliflozin esetén),és a vizelet UACR ≥20 mg/mmol (Magyarországon támogatással 25–75 ml/perc/1,73 m²/*/ bGFR és >3 mg/mmol UACR, valamintRAS-gátló használata esetén írható) vagy szívelégtelenség áll fenn (Magyarországon támogatással csak 40% alatti ejekciós frakció és NYHA II–IV. funkcionális stádiumú tünetekkel járó krónikus szívelégtelenség esetén írható), függetlenül az albuminuria szintjétől.Az SGLT2i bevezetése vagy használata nem teszi szükségessé a CKD-monitorozás gyakoriságának megváltoztatását, illetve az bGFR visszafordítható csökkenése nem jelenti a terápia abbahagyásának szükségességét. SGLT2i kezelés javasolt azoknál a felnőtteknél is, akiknél az bGFR 20–45 ml/perc/1,73 m²/*/közötti és a vizelet UACR
Mineralokortikoid receptor antagonisták (MRA):
Nemszteroid típusú mineralokortikoid receptor antagonistát javasolnak, amely bizonyítottan jótékony hatással van a vesére vagy a szív- és az érrendszerre olyan T2D-s felnőtteknél,akiknéla bGFR >25 ml/perc/1,73 m²/*/, normál szérumkálium-koncentráció és albuminuria (>3 mg/mmol) áll fenn, a RAS-gátló maximális tolerálható dózisának használata ellenére (2A).
A nemszteroid típusú MRA a legmegfelelőbb, olyan T2D-ben szenvedő felnőttek számára is, akiknél nagy a CKD-progresszió és a kardiovaszkuláris események kockázata, valamint tartós albuminuria áll fenn a standard terápia ellenére.Nemszteroid típusú MRA adható a RAS-gátlóhoz és az SGLT2i-hoz a T2D és a CKD kezelésére felnőtteknél.
A hiperkalémia kockázatának csökkentése érdekében válasszunk olyan személyeket, akiknek állandóan normális szérumkálium-koncentrációja van, és ellenőrizze a szérumkálium-szintet rendszeresen a nemszteroid MRA megkezdése után is (2b).A nemszteroid típusú MRA kiválasztásakor előnyben kell részesíteni azokat a szereket, amelyek dokumentált vese- vagy szív- és érrendszeri előnyökkel járnak.A szteroid MRA használható szívelégtelenség, hiperaldoszteronizmus vagy refrakter magas vérnyomás kezelésére, de okozhat hiperkalémiát vagy a glomeruláris filtráció reverzibilis csökkenését, különösen az alacsony GFR-rel rendelkező egyéneknél.
Glukagonszerű peptid-1 receptor agonisták (GLP-1 RA):
Azoknál a T2D-s és CKD-s felnőtteknél, akik nem érték el az egyéni glikémiás célértéket a metformin és az SGLT-2-gátló kezelés esetén, vagy akik nem tudják használni ezeket a gyógyszereket, hosszú hatású GLP-1 RA-t (1B) javasolnak.GLP-1 RA kiválasztásakor előnyben kell részesíteni azokat a szereket, amelyek dokumentált szív- és érrendszeri előnyökkel járnak.
KDIGO holisztikus, lépcsőzetes kezelés
A CKD kezelésének és az egyéni kockázat módosításának holisztikus megközelítése a KDIGO-ajánlás szerint. A kezelés és kockázatcsökkentés első lépése az életmódkezelés: ez magában foglalja az egészséges táplálkozást, a fizikai aktivitást, a dohányzás elhagyását, a megfelelő testsúlykontrollt, mindez megegyezik az ESC-ajánlással. A betegek kockázatbecslését 3–6 havonta újra kell értékelni.
A következő lépés a gyógyszeres kezelés első vonalbeli szintje: folytassuk a megkezdett SGLT-2-gátló kezelést a dialízis vagy a vesetranszplantáció eléréséig, plusz a vérnyomáscélérték
A gyógyszeres kezelés második lépcsőjében (célzott terápiák a szövődmények miatt) kezeljük a magas vércukorszintet, alkalmazzunk GLP-1-RA-kat, ha indikált, és használjuk a KDIGO Diabetes guideline-ját. Használjunk MRA-kat azoknál a betegeknél, akik cukorbetegek vagy egyéb indikáció áll fenn. Az egyéni vérnyomáscélértékek eléréséhez használjunk dihidropirin típusú kalcium-csatorna-blokkolókat és/vagy diuretikumot.Ateroszklerotikus kardiovaszkuláris betegség (ASCVD) esetén használjunk trombocitaaggregáció-gátló szereket. Kezeljük a betegek vérszegénységét, csontbetegségét, káliumeltéréseit és metabolikus acidózisukat, amennyiben szükséges.
Harmadik lépcsőben pedig csökkentsük a magas vérzsírokat,vagy ASCVD esetén alkalmazzunk ezetimibet vagy PCSK-9-inhibitorokat(proprotein convertase subtilisin/kexin type 9). Rezisztens hipertónia eseténadjunk szteroid típusú MRA-kat.
Azt javasolja az irányelv, hogy a magas vérnyomásban és CKD-ben szenvedő felnőtteket 120 Hgmm alatti szisztolés vérnyomás eléréséig kezeljük, a szabályos rendelői vérnyomásméréssel (2B) ellenőrizve. Fontoljuk meg a kevésbé intenzív vérnyomáscsökkentő terápia alkalmazását olyan betegeknél, akiknek gyengeségérzése van, nagy az esés és törések kockázata, nagyon korlátozott a várható élettartam, vagy tünetekkel járó poszturális hipotenzió észlelhető.
A KDIGO irányelvutolsó két fejezetében a GFR-változás okozta farmakokinetikai változások miatti rendszeres gyógyszerellenőrzésre hívják fel a figyelmet, valamint a kontrasztanyagos vizsgálatok megfelelő, körültekintő alkalmazására.Ezenkívül a nefrológiai szakellátásra történőutalás kérdésével foglalkozik és a multidiszciplináris gondozási csoportokhoz való hozzáférés fontosságára is rávilágít. Kiemeli továbbá mint újdonságot a moderntechnológia használatával, digitális platformok és eszközök segítségével a virtuális gondozási csoportok létrehozásának lehetőségét is.
A 2021-ben megjelent magyar szakmai ajánlás szerint, a „Felnőttkori idült vesebetegség diagnózisa és kezelése” című egészségügyi szakmai irányelvvel egybehangzóan, a CKD kezelése az új irányelvekkel továbbra is megegyező RAS-gátló és SGLT-2-gátló bázisterápia, ami speciális esetekben MRA-val vagy diabéteszes betegekben GLP-1-RA-kal kiegészíthető.
Egy új finanszírozási változás is segíti vesevédő kezelés felírását a betegek számára, az idei év elejétől kezdődően ugyanis az SGLT-2-gátlók támogatással írhatók, azon betegek számára, akik bGFR-je 25 és 75 ml/min/1,73 m²/*/ közötti, RAS-gátló kezelés mellettés albuminuriásak (>3 mg/mmol).
Összességében a magas vérnyomás és az idült vesebetegség okozta betegségteher világméretű probléma, azonban a tendenciák megfelelő prevenciós intézkedésekkel és kockázatalapú megközelítéssel nézeteink szerint akár megfordíthatóak is lehetnek.Amagas vérnyomás, a CKD és a szív- és érrendszeri betegségek gyakoribbak, mint a korábbi évtizedekben voltak, és akár már gyermekeknél vagy fiatal felnőtt korban is előfordulhatnak. A megállapított kardiorenális betegség kockázati tényezőinek korai felismerésére kell törekedni a lehetséges károsító hatások megelőzése vagy késleltetése mellett, amelyek akár végzetes következményekkel járhatnak az erekre, a vesékre, a szívre és az agyravonatkozóan – a holisztikus kardiovaszkuláris-renális-metabolikus egészségszemlélet elsajátítása szükséges. A vérnyomás-emelkedés korai diagnózisa és kezelése,illetve a korai vesekárosodás felismerése, amelyet a magas normális albuminuria jelent, fontos feladat minden orvos számára. A kezelés nem különbözik a szív- és vesebetegség előrehaladottabb stádiumaiban sem, de a korábbi kezdet csökkentheti a fennmaradó kardiorenális kockázatot.
A legújabb irányelvek is rávilágítanak arra, hogy minél korábban kezdjük meg a betegeink kezelését és gondozását, annál nagyobb egészségnyereséget tudunk elérni számukra. Az évrőlévre növekvő számú tudományos bizonyítékok is azt mutatják, hogy csak az össztársadalmi szintű beavatkozásoktól várható a kedvezőtlen egészségmutatók javulása.
IRODALOM
- Ndumele CE, Rangaswami J, Chow SL, Neeland IJ, Tuttle KR, Khan SS, et al.Cardiovascular–kidney–metabolic health: a presidential advisory from the American Heart Association. Circulation 2023;148:1606–35. https://doi.org/10.1161/CIR.0000000000001184
- Magyar Nephrológiai Társaság, Nefrológia és Dialízis Tagozat: Egészségügyi szakmai irányelv: A felnőttkori idült vesebetegség diagnózisa és kezelése. Hypertonia és Nephrologia 2021;25(Suppl. 4):S1–S48.
- NCD Risk Factor Collaboration (NCD-RisC). Worldwide trends in hypertension prevalence and progress in treatment and control from 1990 to 2019: a pooled analysis of 1201 population-representative studies with 104 million participants. 2021 Sep 11;398(10304):957–980. DOI: 10.1016/S0140-6736(21)01330-1
- World Health Organisation: Global report on hypertension: the race against a silent killer:2023.https://www.who.int/publications/i/item/9789240081062
- World Health Organisation. Noncommunicable diseases: Risk factors: 2023.https://www.who.int/data/gho/data/themes/topics/topic-details/GHO/ncd-risk-factors
- Group KDIGOKBPW. KDIGO 2021 clinical practice guideline for the management of blood pressure in chronic kidney disease. Kidney Int 2021;99:S1–S87. https://doi.org/10.1016/j.kint.2020.11.003
- Ortiz A, Wanner C, Gansevoort R, Council ERA. Chronic kidney disease as cardiovascular risk factor in routine clinical practice: a position statement by the Council of the European Renal Association. Clin Kidney J 2023;16:403–407. https://doi.org/10.1093/ckj/sfac199
- Staplin N, De la Sierra A, Ruilope LM, Emberson JR, Vinyoles E, Gorostidi M, et al. Relationship between clinic and ambulatory blood pressure and mortality: an observational cohort study in 59 124 patients. Lancet 2023;401:2041–2050. https://doi.org/10.1016/S0140-6736(23)00733-X
- Robinson CH, Chanchlani R. High blood pressure in children and adolescents: current perspectives and strategies to improve future kidney and cardiovascular health. Kidney Int Rep 2022;7:954–970. https://doi.org/10.1016/j.ekir.2022.02.018
- Gerdts E, Izzo R, Mancusi C, Losi MA, Manzi MV, Canciello G, et al. Left ventricular hypertrophy offsets the sex difference in cardiovascular risk (the Campania Salute Network). Int J Cardiol 2018;258:257–261. https://doi.org/10.1016/j.ijcard.2017.12.086
- Gerdts E, Okin PM, De Simone G, Cramariuc D, Wachtell K, Boman K, et al. Gender differences in left ventricular structure and function during antihypertensive treatment: the Losartan intervention for endpoint reduction in hypertension study. Hypertension 2008;51:1109–1114. https://doi.org/10.1161/hypertensionaha.107.107474
- Gerdts E, Wachtell K, Omvik P, Otterstad JE, Oikarinen L, Boman K, et al. Left atrial size and risk of major cardiovascular events during antihypertensive treatment: Losartan Intervention for Endpoint Reduction in Hypertension Trial. Hypertension 2007;49:311–316. https://doi.org/10.1161/01.Hyp.0000254322.96189.85
- Park JB, Schiffrin EL. Small artery remodeling is the most prevalent (earliest?) form of target organ damage in mild essential hypertension. J Hypertens 2001;19:921–930. https://doi.org/10.1097/00004872-200105000-00013
- Vasan RS, Pan S, Xanthakis V, Beiser A, Larson MG, Seshadri S, et al. Arterial stiffness and long-term risk of health outcomes: the Framingham heart study. Hypertension 2022;79:1045–1056. https://doi.org/10.1161/hypertensionaha.121.18776
- Vasan RS, Song RJ, Xanthakis V, Beiser A, DeCarli C, Mitchell GF, et al. Hypertension-mediated organ damage: prevalence, correlates, and prognosis in the community. Hypertension 2022;79:505–515. https://doi.org/10.1161/hypertensionaha. 121.18502
- Group TS. Rapid rise in hypertension and nephropathy in youth with type 2 diabetes: the TODAY clinical trial. Diabetes Care 2013;36:1735–1741. https://doi.org/10.2337/dc12-2420
- Whelton SP, McEvoy JW, Shaw L, Psaty BM, Lima JAC, Budoff M, et al. Association of normal systolic blood pressure level with cardiovascular disease in the absence of risk factors. JAMA Cardiol 2020;5:1011–1018. https://doi.org/10.1001/jamacardio.2020.1731
- Ruilope LM, Ortiz A, Lucia A, Miranda B, Alvarez-Llamas G, Barderas MG, et al. Prevention of cardiorenal damage: importance of albuminuria. Eur Heart J 2023;44: 1112–1123. https://doi.org/10.1093/eurheartj/ehac683
- Agbaje AO. Arterial stiffness precedes hypertension and metabolic risks in youth: a review. J Hypertens 2022;40:1887–1896. https://doi.org/10.1097/HJH.0000000000003239
- Ruilope LM, Ortiz A, Ruiz-Hurtado G. Hypertension and the kidney: an update. European Heart Journal 2024;45:1497–1499. https://doi.org/10.1093/eurheartj/ehad896
- European Society of Cardiology. Guidelines for the management of elevated blood pressure and hypertension. European Heart Journal 2024;45:3912–4018.https://doi.org/10.1093/eurheartj/ehae178
- Brown JM, Siddiqui M, Calhoun DA, Carey RM, Hopkins PN, Williams GH, et al. The unrecognized prevalence of primary aldosteronism: a cross-sectional study. Ann Intern Med 2020;173:10–20. https://doi.org/10.7326/m20-0065
- Oparil S, Acelajado MC, Bakris GL, Berlowitz DR, Cífková R, Dominiczak AF, et al. Hypertension. Nat Rev Dis Primers 2018;4:18014. https://doi.org/10.1038/nrdp. 2018.14
- Nazarzadeh M, Bidel Z, Canoy D, Copland E, Bennett DA, Dehghan A, et al. Blood pressure-lowering treatment for prevention of major cardiovascular diseases in people with and without type 2 diabetes: an individual participant-level data meta-analysis. Lancet Diabetes Endocrinol 2022;10:645–654. https://doi.org/10.1016/s2213-8587(22) 00172-3
- Beddhu S, Chertow GM, Greene T, Whelton PK, Ambrosius WT, Cheung AK, et al. Effects of intensive systolic blood pressure lowering on cardiovascular events and mortality in patients with type 2 diabetes mellitus on standard glycemic control and in those without diabetes mellitus: reconciling results from ACCORD BP and SPRINT. J Am Heart Assoc 2018;7:e009326. https://doi.org/10.1161/jaha.118.009326
- Malhotra R, Nguyen HA, Benavente O, Mete M, Howard BV, Mant J, et al. Association between more intensive vs less intensive blood pressure lowering and risk of mortality in chronic kidney disease stages 3 to 5: a systematic review and meta-analysis. JAMA Intern Med 2017;177:1498–505. https://doi.org/10.1001/jamainternmed.2017.4377
- Lv J, Ehteshami P, Sarnak MJ, Tighiouart H, Jun M, Ninomiya T, et al. Effects of intensive blood pressure lowering on the progression of chronic kidney disease: a systematic review and meta-analysis. CMAJ 2013;185:949–957. https://doi.org/10.1503/cmaj. 121468
- Cheung AK, Rahman M, Reboussin DM, Craven TE, Greene T, Kimmel PL, et al. Effects of intensive BP control in CKD. J Am Soc Nephrol 2017;28:2812–2823. https://doi.org/10. 1681/asn.2017020148
- Ku E, McCulloch CE, Inker LA, Tighiouart H, Schaefer F, Wühl E, et al. Intensive BP control in patients with CKD and risk for adverse outcomes. J Am Soc Nephrol 2023;34:385–393. https://doi.org/10.1681/asn.0000000000000072
- Herrington WG, Staplin N, Wanner C, Green JB, Hauske SJ, Emberson JR, et al. Empagliflozin in patients with chronic kidney disease. N Engl J Med 2023;388:117–127. https://doi.org/10.1056/NEJMoa2204233
- Heerspink HJL, Stefánsson BV, Correa-Rotter R, Chertow GM, Greene T, Hou F-F, et al. Dapagliflozin in patients with chronic kidney disease. N Engl J Med 2020;383: 1436–1446. https://doi.org/10.1056/NEJMoa2024816
- Lewis EJ, Hunsicker LG, Clarke WR, Berl T, Pohl MA, Lewis JB, et al. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes. N Engl J Med 2001;345:851–860. https://doi.org/10.1056/ NEJMoa011303
- European Society of Hypertension clinical practice guidelines for the management of arterial hypertension 2024. European Journal of Internal Medicine 2024;126:1–15. https://doi.org/10.1016/j.ejim.2024.05.033
KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney International 2024;105(Suppl 4S):S117–S314. KDIGO-2024-CKD-Guideline.pdf
a szerző cikkei




