A leggyakoribb mozgászavarok differenciáldiagnosztikája
A neurológiai eredetű mozgászavarok az idősödő társadalomban egyre nagyobb kihívást jelentenek. Annak ellenére, hogy viszonylag ritka előfordulásúak, a prevalenciaadatok alapján a legtöbb egészségügyi szolgáltató a praxisa során találkozni fog ezekkel. A betegek életminőségét jelentősen befolyásoló kórállapotok felismerése számos differenciáldiagnosztikai és terápiás nehézséget okozhat, illetve kezelésük sok esetben multidiszciplináris csapatmunkát és speciális szaktudást igényel. Ezt a munkát segítik a folyamatosan fejlesztett szakmai irányelvek, nemzetközi konzorciumok és a szakmai szervezetek által szervezett folyamatos továbbképzések. Jelen összeállításban a leggyakoribb kórképek differenciáldiagnosztikai szempontjait ismertetjük.
Az extrapyramidalis kórképek színes és igen változatos klinikai megjelenési formái miatt diagnosztizálásuk és kezelésük kiemelt szaktudást, nagy gyakorlatot, multidiszciplinális megközelítést, valamint csapatmunkát igényel. A pontos kórismézéshez sok esetben elengedhetetlen bizonyos speciális labor- és képalkotó diagnosztikai vizsgálatok elvégzése is. Napjainkban a fenotípuson alapuló klinikai felosztást sok esetben felváltja a genetikai klasszifikáció, amelynek komplexitása miatt elkerülhetetlenné válik a klinikai genetikus szakorvos bevonása a betegellátásba.
PARKINSON-KÓR
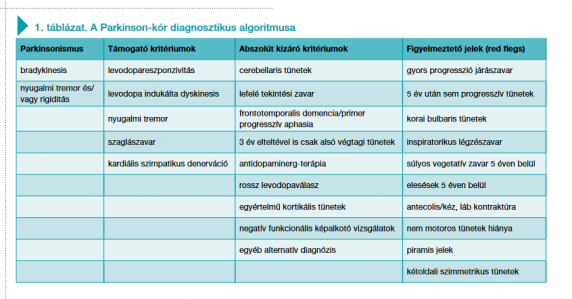
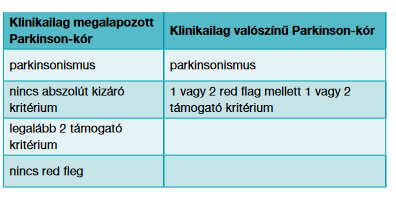
A neurológiai eredetű mozgászavarok közül messze a leggyakoribb a tremor. A tremort gyakran (és tévesen) a Parkinson-kórral teszik egyenértékűvé, ezáltal sok diagnosztikus és terápiás tévedést előidézve. A Parkinson-kór diagnosztizálása sajnálatosan a mai napig csak a megjelenő klinikai tüneteken alapul. Egyelőre nem ismerünk olyan vizsgálómódszert, amely minden kétséget kizárólag, nagy szenzitivitással és specificitással igazolná a kórkép fennállását. A jellegzetes motoros (mozgáslelassulás, izommerevség, nyugalmi tremor) eltérések általában az 50–60. életév között jelentkeznek, de bizonyos nem motoros tünetek (obstipáció, depresszió, alvászavar, szaglászavar stb.) már évtizedekkel hamarabb megjelenhetnek. Tekintettel arra, hogy a parkinsonismus tünetei sok más mozgászavarral mutathatnak átfedést, a betegség kórismézésére több diagnosztikus kritériumrendszert is létrehoztak. Ezek közül a legújabb és talán a legmegbízhatóbb a Movement Disorders Society által kidolgozott klinikai diagnosztikai algoritmus (1), amelynek alapja a parkinsonismus igazolása mellett a támogató és a kizáró kritériumok azonosítása (1. táblázat). Ennek a rendszernek az alkalmazásával jelentősen javítható a diagnosztikus pontosság. Bár a nemzetközi ajánlásoknak még nem része a kórkép alapjául szolgáló, kóros szerkezetű és tulajdonságú α-synuclein jelenlétének laboratóriumi kimutatása, ennek ellenére ez a vizsgálat számos helyen már elvégezhető a világban, megkönnyítve a kórkép azonosítását. Ugyanúgy a genetikai vizsgálatok sem tartoznak az ajánlott módszerek közé, mégis egyre inkább általánossá válik a ritka familiáris formák génjei mellett (PARK2, DJ-1, PINK, LRRK2) a gyakoribb genetikai rizikófaktorok (GBA) vizsgálata is (2).
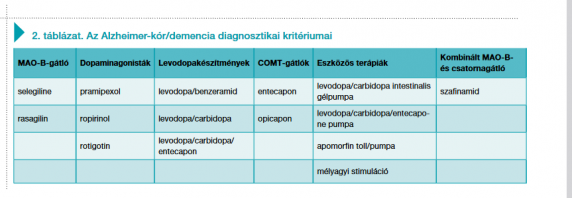
A klinikai diagnózis felállítását követően megkezdett tüneti terápia alapja a dopaminrendszer működésének helyreállítása. Erre a célra szolgálnak a MAO-B-gátlók, a dopaminagonisták, illetve a különböző levodopakészítmények (3). Előrehaladott stádiumban, amikor a gyógyszeres kezeléssel már nem érhető el megfelelő mozgásteljesítmény és életminőség-javulás, a mozgászavarközpontokban elvégzett eszközös terápiák (mélyagyi stimuláció, gyógyszeradagoló pumpák) nyújthatnak segítséget a betegeknek a mozgásteljesítményük javítására (2. táblázat) (4). Sajnos egyelőre a betegség lefolyását módosító vagy oki terápia nem áll rendelkezésünkre, bár az α-synuclein-ellenes immunterápiával kapcsolatban több nagy nemzetközi klinikai vizsgálat is folyamatban van.
Megjegyzendő, hogy a parkinsonismus több kórképben megjelenhet, amelyek hasonlóságot mutathatnak a Parkinson-kórhoz, de számos egyéb tünet utal arra, hogy más betegséggel állunk szemben (red fleg jelek). Amennyiben a parkinsonismus tünetei mellé cerebellaris jelek vagy éppen vegetatív zavar (ortostaticus hypotensio vagy vizeletinkontinencia) társulnak, az inkább multisystemás atrophiára utal. Amennyiben a parkinsonismus mellé vertikális szemmozgászavar vagy tartási instabilitás/gyakori elesések társulnak, akkor inkább progresszív supranuclearis bénulás a valószínű diagnózis. A kórlefolyás során hamar jelentkező vizuális hallucinációk pedig Diffúz Lewy-testes demenciára utalhatnak. Ezeknek a kórképeknek az elkülönítése az idiopathiás Parkinson-kórtól azért fontos, mert a prognózisuk sajnálatos módon rosszabb, és ezek a betegek a szokásos dopaminergterápiákra is rosszabbul reagálnak.
ESSZENCIÁLIS TREMOR
Az esszenciális tremor az egyik leggyakoribb mozgászavar, amelynek a Parkinson-kórtól való elkülönítése kiemelten fontos, hiszen alapjaiban más kezelést igényel. Míg Parkinson-kórban jellegzetesen nyugalmi tremor jelentkezik, addig esszenciális tremorban a remegés inkább akciós és/vagy posturalis jellegű. Éppen ezért panaszkodnak a betegek arra, hogy az étkezés, az ivás vagy éppen az írás vált nehezítetté a tünetek megjelenését követően. Ezzel szemben nyugalomban nincs mozgászavaruk. Ugyancsak jellegzetes, hogy ebben a kórállapotban a fejtremor vagy a laringeális tremor gyakran fordul elő, míg ezek általában nem észlelhetők Parkinson-kórban. Maga a betegség autoszomális domináns módon öröklődik, de egyértelműen a betegséghez köthető gén(ek) ez ideig még nem ismert(ek). A tremor általában a 20-as és az 50-es életévekben erősödik fel olyan mértékben, hogy a beteg számára panaszokat okoz (5). A kórisme felállításához a spirálrajzoláson túl a kézírás vizsgálata vagy a pohárból való ivás is felhasználható.
A limitált számú és effektivitású gyógyszeres kezelés mellett (propanolol, topiramat, primidon), bizonyos esetekben mélyagyi stimulációs műtét is szükségessé válhat, ahol a thalamus speciális magcsoportjának nagy frekvenciás stimulációja a tüneteket enyhítheti (6).
HUNTINGTON-KÓR
A Huntington-kór agy autoszomális, domináns módon öröklődő genetikai betegség, amely jellemzően a felmenők között is azonosítható (legtöbbször pozitív a családi anamnesis). A mutáció a 4 kromoszómán található IT-15 gén CAG ismétlődés számának növekedéséből áll. A mozgászavar, amely legtöbbször distalis, random mozgásokat mutató chorea, 40-50 éves kor körül kezdődik, de ezt sok évvel megelőzheti a magatartás-változás, illetve a későbbiekben, a kórkép előrehaladtával ezek mellé társuló jelentős neurokognitív zavar is (7). A mozgászavar a későbbiekben már nem tisztán chorea, hanem legtöbbször kombinálódik más kényszermozgásokkal. A jellegzetes tünetek, a családi halmozódás a kórkép diagnosztizálását megkönnyíti. A kórkép teljes penetranciájú, vagyis azok, akik hordozzák a mutációt, mindenképpen megbetegednek, és a tünetkezdet többé-kevésbé korrelál a genetikai vizsgálat során kimutatott ismétlődésszámmal.
Sajnos jelenleg a betegség lefolyását módosító oki terápia nem áll rendelkezésünkre a betegség kezelésére, habár genetikai alapú terápiákkal a világban több nagy klinikai vizsgálat is folyik (8). Oki terápia hiányában tüneti kezelés javasolható, amely elsősorban a túlmozgások, illetve a pszichés tünetek kezelésére szorítkozik. Kiemelném, hogy Huntington-kór gyanúja esetén, genetikai tanácsadást követően, a diagnosztikus vizsgálat mellett prenatális genetikai vizsgálatra Magyarországon is van lehetőség.
FOKÁLIS DYSTONIÁK
Ebbe a betegségcsoportba azok a kórképek tartoznak, ahol egy vagy több testtájékon levő izmok akaratlan, kóros összehúzódása jelentkezik, ami a kóros mozgást vagy testtartást eredményezi. Ennek egyik példája a szemhéjgörcs vagy blepharospasmus. Ekkor a m. orbicularis oculi tartós és akaratlan izom-összehúzódása gyakori pislogást vagy a szemek becsukódását eredményezheti, de súlyos esetben funkcionális vakságot is okozhat. A myasthenia gravisra jellemző ptosistól való elkülönítésben segítségül szolgálhat az a megfigyelés, hogy szemhéjgörcsben az alsó szemhéj is koncentrikusan összehúzódik, míg ez ptosis esetén nem figyelhető meg. Az életminőséget jelentősen rontó kórállapot kezelésére a centrumokban alkalmazott rendszeres lokális botulinumtoxin-infiltráció szolgál.
Ugyancsak a fokális dystoniák csoportjába tartozik a cervicalis dystonia vagy ferdenyakúság. Ebben az esetben a beteg feje a középvonalból akaratlanul és tartósan elmozdul, sokszor laterális vagy torziós irányban. Ez kezdetben akaratlagosan leküzdhető, a normál állapot visszaállítható, de a későbbiekben fixálódhat is. A tartós izom-összehúzódás fájdalmas lehet, és a beteg mobilitását korlátozhatja. Ebben az esetben is segítséget jelenthet a tünettan alapján azonosított és kórosan aktiválódott nyaki izmok ultrahangvezérelt botulinumtoxin-infiltrációja.
WILSON-KÓR
A Wilson-kór egy autoszomális, recesszív módon öröklődő rézanyagcsere-betegség. A réztranszport-protein hiánya miatt a réz lerakódik a parenchimalis szervekben (így többek között az agyban, a szemben, illetve a májban), a károsodásukat előidézve. A réztranszport-deficiencia súlyosságától függően eltérő klinikai tünetek jelentkeznek. Legsúlyosabb esetekben már fiatalkorban jelentkező májelégtelenség, enyhébb esetekben későbbi életkorban kezdődő mozgászavar vagy pszichiátriai tünetek állhatnak a tünetek előterében. A fiatalkorban észlelt májfunkciós eltérések mellett a koponya-MRI-felvételeken kimutatható rézlerakódás is felvetheti a Wilson-kór gyanúját, amelyet genetikai vizsgálattal is meg kell erősíteni (9).
A kórkép tüneti kezelésére a rézszegény diéta mellett alkalmazott kelátképzők adásával érhető el a szabadréz-szint csökkenése, és ezáltal a klinikai tünetek javulása. Tekintettel a változatos klinikai fenotípusra, az érintett szakterületek bevonása a betegek kezelésébe mindenképpen szükséges lehet. Bizonyos válogatott esetekben oki terápiaként a májtranszplantáció is szükségessé válhat.
FRIEDREICH-ATAXIA
A veleszületett ataxiák egy rendkívül heterogén betegcsoport, amelyek mindegyikében vezető tünet a járászavar, illetve a végtagok koordinációs zavara. Az ataxia mellett megjelenő tünetek rendkívüli változatossága igen nehézzé teszi a kórkép pontos diagnosztizálását. A legtöbb típusra jellemző a koponya-MRI-felvételeken észlelhető, különböző fokú cerebellaris és/vagy agytörzsi/hemispherialis atrophia. A betegség legtöbbször genetikailag meghatározott, de a genetikai diagnózist nehezíti az, hogy a számos génben nagy számban észlelt genetikai eltérések döntő többségének kóroki szerepe még nem került egyértelműen megerősítésre.
Az ebbe a csoportba tartozó és relatíve gyakran előforduló Friedreich-ataxia egy autoszomális recesszív betegség, amelynek oka az FRDA gén első intronjában található GAA-ismétlődés hosszának növekedése. A tünetek általában fiatalfelnőtt-korban kezdődnek járászavarral és végtagügyetlenséggel, amihez a későbbiekben diabetes, gerincdeformitás és cardiomyopathia is társulhat (10). Differenciáldiagnosztikai szempontból az életkor miatt a sclerosis multiplexet kell megemlíteni, ahol a Friedreich-ataxiával ellentétben jellegzetes fehérállományi léziók láthatók az MRI-felvételeken. A kórkép kezelésére sajnos csak rendkívül szerény lehetőségek állnak rendelkezésünkre, és azok is elsősorban tüneti hatásúak. A betegek életét elsősorban a kialakuló társuló diabetes mellitus és a cardiomyopathia veszélyezteti. Ezek kezelése a társszakmák bevonását igényli.
MOZGÁSZAVARRAL FOGLALKOZÓ KÖZPONTOK ÉS SZAKMAI SZERVEZETEK
A rendkívül heterogén betegségcsoportok diagnosztikai és kezelési nehézségei miatt vált szükségessé a specializált centrumok és szakmai szervezetek létrehozása mind nemzetközi, mind hazai szinten. Magyarországon a mozgászavarok kezelése jellemzően a négy egyetemi centrum mellett nagyobb kórházak neurológiai osztályain folyik, bár ezek nem mindegyik esetben fedik le a jelenleg elérhető teljes diagnosztikai és terápiás palettát. Éppen ezért rendkívül fontosnak tartjuk a mozgászavarokkal kapcsolatos folyamatos továbbképzéseket, az elérhetővé váló újabb és újabb diagnosztikus és terápiás eljárások mihamarabbi hazai bevezetését is.
Annak ellenére, hogy a legtöbb betegségnek van önálló szakmai képviselete nemzetközi szinten (European Huntington’s Disease Network, Autosomal Recessive Cerebellar Ataxias Registry stb.), a legjelentősebb szakmai szervezet az amerikai Movement Disorders Society, ill. az európai European Academy of Neurology Movement Disorders Panelja (11). Hazai kollégák a két nagy társaság mellett több önálló társaság munkájában is aktívan részt vesznek. Idehaza az 1999-ben megalakított Magyar Tudományos Parkinson Társaság döntően a Parkinson-kórral kapcsolatos továbbképzéseket és szakmai egyeztetéseket végzi. Emellett az egyéb mozgászavarok megjelenési formáival a Magyar Klinikai Neurogenetikai Társaság és a Magyar Humángenetikai Társaság is foglalkozik (12).
ÖSSZEFOGLALÁS
A genetikai vizsgálatok elterjedésével és újabb technológiai fejlesztésekkel a neurológiai eredetű mozgászavarok diagnosztikája a klinikai alapokról fokozatosan áttevődik genetikai alapokra. Ennek következtében nyilvánvalóvá vált, hogy számos tünet, ill. eltérés nemcsak egy betegséghez tartozhat, hanem több más kórképben is megjelenhet, ezáltal megnehezítve a klinikai diagnózis felállítását. A genetikai eltérések azonosítása viszont új utakat nyitott meg a személyre szabott, célzott terápiák fejlesztéséhez. Ez a korszakváltás jelenleg is zajlik. Ebből a szempontból is kiemelten fontosnak tartjuk a neurológusok folyamatos továbbképzését, a mozgászavarcentrumok szakmai és infrastrukturális fejlesztését, valamint a már meglévő nemzetközi kollaborációk továbbfejlesztését. Az ehhez szükséges személyi és tárgyi feltételek biztosítása elsősorban az adott intézmény feladata, míg a pénzügyi források rendelkezésre bocsátása már szakmapolitikai kompetencia. A hazai orvostársadalomnak mindent el kell követnie, hogy erre a rendkívül gyors fejlődésre minden szinten szakmailag felkészüljünk, hogy a betegeink minél hamarabb részesülhessenek a rendkívül gyors fejlődés eredményeiből.
IRODALOM
- Postuma RB, Berg D, Stern M, et al. MDS clinical diagnostic criteria for Parkinson’s disease. Mov Disord 2015;30(12):1591–1601.
- Funayama M, Nishioka K, Li Y, Hattori N. Molecular genetics of Parkinson’s disease: Contributions and global trends. J Hum Genet 2023;68(3):125–130.
- Pringsheim T, Day GS, Smith DB, et al. Dopaminergic Therapy for Motor Symptoms in Early Parkinson Disease Practice Guideline Summary: A Report of the AAN Guideline Subcommittee. Neurology 2021;97(20):942–957.
- Deuschl G, Antonini A, Costa J, et al. European Academy of Neurology/Movement Disorder Society-European Section Guideline on the Treatment of Parkinson’s Disease: I. Invasive Therapies. Mov Disord 2022;37(7):1360–1374.
- Pan MK, Kuo SH. Essential tremor: Clinical perspectives and pathophysiology. J Neurol Sci 2022;435:120198.
- Frei K, Truong DD. Medications used to treat tremors. J Neurol Sci 2022;435:120194.
- Ajitkumar A, Jesus OD. Huntington Disease. In: StatPearls. Publishing; 2023 Aug.
- Fritz NE, Busse M, Muratori LM, et al. An MDS Evidence-Based Review on Treatments for Huntington’s Disease. Mov Disord 2022;37(7):1566–1567.
- Kasztelan-Szczerbinska B, Cichoz-Lach H. Wilson’s Disease: An Update on the Diagnostic Workup and Management. J Clin Med 2021;10(21):5097.
- 10. Keita M, McIntyre K, Rodden LN, Schadt K, Lynch DR. Friedreich ataxia: clinical features and new developments. Neurodegener Dis Manag 2022;12(5):267–283.
11. Bassetti CL. European Academy of Neurology 2019–2022. Eur J Neurol 2022;29(9):2567–2571.
a szerző cikkei


