A T-sejtektől a D-vitaminig
A szklerózis multiplex kialakulásához - vagyis az idegsejtek szigetelését biztosító mielinhüvely gyulladásásához és pusztulásához - valószínűleg több tényező együttes hatása szükséges. A jelenlegi terápiás eszköztárat az interferon béta-1a, a glatiramer-acetát, a mitoxantrone és a natalizumab alkotja. Írásunkban autoimmun megközelítésből próbálunk a jövőbe látni.
Optimista megközelítésben az, hogy az autoimmunitásnak számos bonyolult oka lehet, akár jó hírként is felfogható, hiszen ez sok terápiás célpontot jelent. A kezelés kulcsa valószínűleg nem egy adott út teljes gátlása lesz, hanem a számos pontot kismértékben érintő beavatkozás.
A tolerancia visszaállítása
Az autoimmunitás egyik kulcsmozzanata az, hogy az immunsejtek érése során az autoreaktív T- és B-sejtek eltávolítása (az úgynevezett centrális, illetve a perifériás tolerancia) zavart szenved, nem teljes körű. Ha ezt ki lehetne védeni, akkor nem alakulna ki autoimmunitás. Ennek a megközelítésnek a hátránya, hogy többet árthat, mint amennyit használ.
DNS-vakcina
Ezek a gyógyszerjelöltek a mielinhüvely egyik alkotóelemét, a mielinbázikus proteint (MBP) - szklerózis multiplexben (SM) az autoimmunitás e fehérje ellen irányul - vagy annak egy darabját kódoló plazmidok. Az immunfolyamatokban az antigénprezentáló sejtek MHC-molekulái által bemutatott MBP-fragmentumokat felismerő receptorokat termelő T-sejtek játsszák a főszerepet. Az MBP-t vagy annak egy darabját kódoló DNS ismételt (6 havonkénti, intravénás) bejuttatásától azt várják, hogy elnyomja az MBP elleni immunválaszt. Jelenleg humán fázis II-III. vizsgálatok folynak velük.
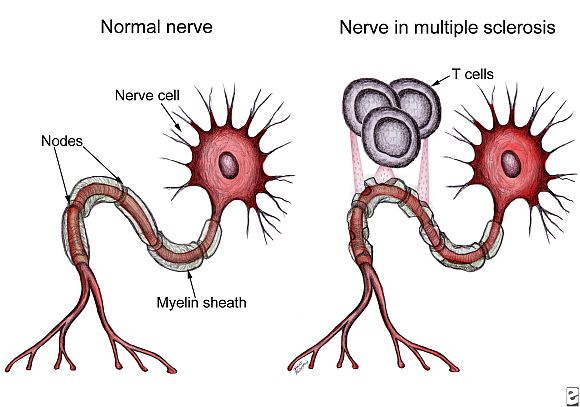
Küzdelem a T-sejtekkel
A regulációs T-sejtek (Treg) működését fokozó szereket is klinikai vizsgálatokban tesztelik. Ilyen például a FoxP3 fehérje, illetve a CD28 receptoron ható CTLA4 immunglobulin (szelekív kostimuláció modulátor). E megközelítés alapján is dolgoznak vakcinaszerű elgondolásokon: a nem megfelelően működő Treg-sejtek egyik, az adott betegségben gyakrabban jelen lévő receptorát gátolná egy peptid.
További támadási pont a T-sejtek célszövetbe való eljutásának megakadályozása. Így hat például a már piacon lévő natalizumab, amely az a4b1 integrinhez kapcsolódva gátolja meg a limfociták kijutását az érpályából.
Baktériumok bevetésen
A normál bélflóra részét képező szegmentált filamentózus baktériumok (SFB) speciális segítő (helper) T-sejtek, a Th17 limfociták megjelenését idézik elő baktériummentes környezetben tartott egerekben - igazolta párhuzamosan két munkacsoport is a közelmúltban (Cell, 2009 Oct 30;139(3):485-98; Immunity, 2009 Oct 16;31(4):677-89).
A Th17 sejtek túlműködésének - a citokinek fokozott termelése révén - szerepet tulajdonítanak egyes autoimmun betegségek, köztük a szklerózis multiplex kialakulásában. Ezt támasztja alá, hogy a Th17-hiányos állatokban nem alakulnak ki autoimmun kórképek, vagy lefolyásuk lényegesen enyhébb. Az SFB-vel kezelt állatokat egyébként később nem betegítette meg a rágcsálókban E. coli-hoz hasonló fertőzést okozó Citrobacter rodentium. Úgy tűnik, hogy ilyen, az immunrendszer érését és válaszkészségét előmozdító mechanizmussal a több száz fajból álló bélflóra tagjai közül csak az SFB rendelkezik - talán azért, mert a patogén baktériumokhoz hasonlóan meg tud tapadni a bélhámsejtek felszínén.
Néhány hónapon belül az SFB DNS-ének teljes szekvenciája ismert lesz. Így a kutatók kezébe kerül az általa kódolt fehérjekészlet is. A Th17-sejtek képződéséért/aktivációjáért felelős protein azonosításával gyógyszercélponthoz juthatunk.
A high-tech elgondolások mellett vannak egyszerűbb, de biztonságosabb próbálkozások is. Ígéretesnek tűnik például a sztatinok immunmoduláló hatása.
D-vitamin pro és kontra
Gyűlnek az adatok a D-vitamin szerepéről is. A Koppenhágai Egyetem kutatói például igazolták, hogy kulcsszerepet játszik a védekezőképesség aktiválásában (Nat Immunol, 2010 Apr;11(4):344-9.). Úgy találták ugyanis, hogy naiv T-sejtekben csak igen kis mennyiségben van jelen a T-sejt antigénreceptora révén létrejövő immunválaszért felelős jelátviteli út kulcsszereplője, a foszfolipáz-C (PLC) gamma1 enzim, valamint a D-vitamin-receptor. Kísérleteik során igazolták, hogy a PLC-expresszióhoz - következésképpen a T-sejt receptoron keresztüli aktivációjához - D-vitaminra és D-vitamin-receptorra van szükség.
Egy másik munkacsoport eredményei szerint viszont a napfény ultraibolya (UV-) sugárzása nem a D-vitamin-szintézis fokozása révén gyakorol jó hatást az SM-re (Proc Natl Acad Sci USA, 2010 Mar 22). A kutatók SM-hez hasonló elváltozást hoztak létre egerekben fehérjeinjekcióval; az állatok egy részét UV-sugárzásnak tették ki a károsító hatás előtt és után, másik részük csak az injekciót kapta meg, UV-kezelés nélkül. A sugárzásban is részesülő egerekben sokkal kevésbé mutatkoztak az SM-szerű betegség tünetei, mint a másik csoportban, noha a sugárzás hatására nem emelkedett jelentősen az állatok vérében a D-vitamin szintje. Egy másik kísérletben az egerek egyes csoportjai különböző dózisú D-vitamint kaptak, de UV-sugárzást nem alkalmaztak. A D-vitamin nem befolyásolta sem a betegség kezdetét, sem súlyosságát, sem előrehaladását.
A szélességi fok hipotézisMindeddig azt feltételezték, hogy a trópusokon azért fordul elő ritkán az SM, mert a napfény UV-sugárzásának hatására nagy mennyiségű D-vitamin szintetizálódik az emberek szervezetében. Ezt támasztotta alá az is, hogy Európa és Észak-Amerika északi területein gyakoribb a betegség, mint délebbre. Közvetlen ok-okozati kapcsolatot azonban soha nem sikerült igazolni a D-vitamin-hiány és az SM között. Emellett a korábbi állatkísérletekben, amelyekben SM-szerű betegségben szenvedő egereknek D-vitamint adtak, csak toxikus mennyiségű D-vitaminnak volt terápiás hatása. |
TünettanAz SM tünetei alapvetően a sérült idegi területet tükrözik. Az érző idegek károsodása megnyilvánulhat zsibbadás, fülcsengés, fájdalom, égető érzés, viszketés, arcideggel kapcsolatos fájdalom, látászavar formájában. A motoros idegekkel kapcsolatos tünetek közé sorolható a beszédhiba, a fizikai gyengeség, a remegés, a nehezített járás, az összehangoltság hiánya, a székrekedés, a vizelettartási problémák. A pszichés tünetek kedélyállapot-ingadozás, depresszió és a felismerő képesség gyengülésének képében jelentkezhetnek. |




